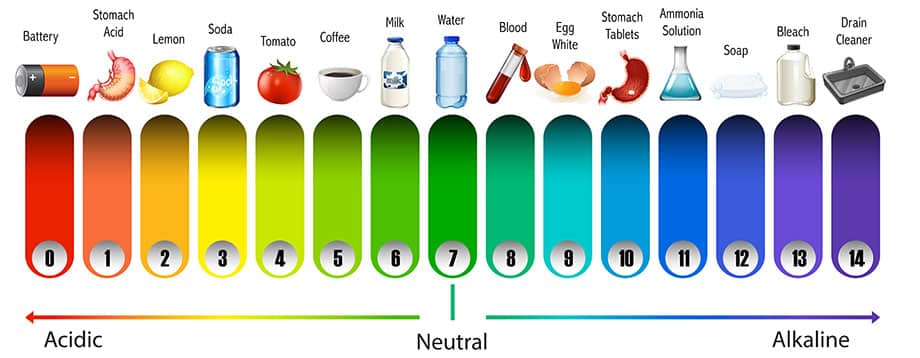
ค่าความเป็นกรดด่างคือการวัดความเข้มข้นของไฮโดรเจนไอออน ซึ่งเป็นระดับกรดหรือด่างของสารละลาย ซึ่งเรียกว่าค่าพีเอช (pH) มาตราส่วนจะอยู่ในช่วงตั้งแต่ 0 ถึง 14
สารละลายที่มีค่า pH น้อยกว่า 7 จะเป็น “กรด” ในขณะที่สารละลายที่มีค่ามากกว่า 7 เป็น “ด่าง” ในขณะระดับพีเอชเท่ากับ 7.0 ที่ 25°C ถูกกำหนดให้เป็น “เป็นกลาง“
เนื่องจากความเข้มข้นของ H3O+ เท่ากับความเข้มข้นของ OH− ในน้ำบริสุทธิ์ กรดที่แรงมากอาจมี pH เป็นลบ ในขณะที่เบสที่แรงมากอาจมี pH มากกว่า 14 ได้ (ไม่ได้จำกัดแค่ 0-14 เท่านั้น)
ในชีวิตประจำวันของเรา พบเครื่องดื่มจำนวนมากที่มีค่าพีเอชที่ต่างกันเช่นน้ำเป็นสารที่เป็นกลาง โซดาและกาแฟมักมีความเป็นกรด
ซึ่งค่าความเป็นกรด – ด่างเป็นคุณสมบัติที่สำคัญ เนื่องจากมีผลต่อปฏิกิริยาของสารระหว่างกันและกับร่างกายของเรา ในทะเลสาบและมหาสมุทรของเรา ค่าพีเอชเป็นตัวกำหนดว่าสิ่งมีชีวิตใดสามารถอยู่รอดในน้ำได้

สมการ pH
สมการสำหรับการคำนวณค่า pH ถูกเสนอในปี 1909 โดยนักชีวเคมีชาวเดนมาร์ก Søren Peter Lauritz Sørensen:
pH = -log[H+]
โดยที่ log คือลอการิทึมฐาน 10 และ [H+] หมายถึงความเข้มข้นของไฮโดรเจนไอออนในหน่วยของโมลต่อสารละลายลิตร
คำจำกัดความใหม่ของ pH ตามมาตรฐาน IUPAC
International Union of Pure and Applied Chemistry (IUPAC) มีมาตราส่วน pH ที่แตกต่างกันเล็กน้อยซึ่งอิงตามการวัดทางไฟฟ้าเคมีของสารละลายบัฟเฟอร์มาตรฐาน โดยพื้นฐานแล้วคำจำกัดความใช้สมการ:
pH = -log aH+
โดยที่ aH+ หมายถึงกิจกรรมของไฮโดรเจน ซึ่งเป็นความเข้มข้นของไฮโดรเจนไอออนในสารละลายที่มีประสิทธิผล ซึ่งอาจจะแตกต่างจากความเข้มข้นที่แท้จริงเล็กน้อย มาตราส่วนพีเอชของ IUPAC ยังรวมถึงปัจจัยทางอุณหพลศาสตร์ ซึ่งอาจส่งผลต่อค่า pH

pH ย่อมาจาก
คำว่า “pH” มาจากคำภาษาเยอรมัน “potenz” ซึ่งแปลว่า “กำลัง” รวมกับ H ซึ่งเป็นสัญลักษณ์ธาตุของไฮโดรเจน ดังนั้น pH จึงเป็นตัวย่อของ “พลังของไฮโดรเจน”
ตัวอย่างค่า pH ของสารเคมีทั่วไป
เราทำงานกับกรดหลายชนิด (พีเอชต่ำ) และเบส (พีเอชสูง) ทุกวัน ตัวอย่างค่าพีเอชของสารเคมีในห้องปฏิบัติการและผลิตภัณฑ์ในครัวเรือน ได้แก่
- 0: กรดไฮโดรคลอริก
- 2.0: น้ำมะนาว
- 2.2: น้ำส้มสายชู
- 4.0: ไวน์
- 7.0: น้ำบริสุทธิ์ (เป็นกลาง)
- 7.4: เลือดมนุษย์
- 13.0: น้ำด่าง
- 14.0: โซเดียมไฮดรอกไซด์
ของเหลวบางชนิดไม่มีค่า pH
ค่า pH มีความหมายเฉพาะในสารละลายที่เป็นน้ำ (มีน้ำเป็นส่วนประกอบ) สารเคมีหลายชนิดรวมทั้งของเหลวไม่มีค่าพีเอช หากไม่มีน้ำแสดงว่าไม่มี pH ตัวอย่างเช่นน้ำมันพืช น้ำมันเบนซิน หรือแอลกอฮอล์บริสุทธิ์

วิธีวัดค่า pH
กระดาษทดสอบกรด-ด่าง
การวัดค่า pH แบบหยาบสามารถทำได้โดยใช้กระดาษลิตมัสหรือกระดาษ pH ชนิดอื่นที่ทราบกันว่าเปลี่ยนสีที่แน่นอน
ตัวชี้วัดและกระดาษวัดค่า pH ส่วนใหญ่มีประโยชน์เพียงเพื่อบอกว่าสารเป็นกรดหรือด่าง หรือเพื่อระบุค่า pH ภายในช่วงแคบเท่านั้น ไม่เหมาะสำหรับกรณีที่ต้องการความแม่นยำ


กระดาษทดสอบ pH
สินค้าแบรนด์ German คุณภาพสูงขายราคาถูก มีใบรับรอง Certificate of Analysis จากผู้ผลิต ดูรายละเอียดเพิ่มเติม
พีเอชมิเตอร์
การวัดที่แม่นยำยิ่งขึ้นทำได้โดยใช้เครื่องมือทางอิเล็กโทรนิกส์ที่ใช้หลักการทางไฟฟ้าเคมีเรียกว่างเครื่องวัดค่า pH Meter ทำงานโดยการวัดความต่างศักย์ระหว่างอิเล็กโทรดไฮโดรเจนกับอิเล็กโทรดมาตรฐาน
มีสินค้าหลากหลายให้เลือกได้แก่แบบปากกา แบบตั้งโต๊ะ แบบใช้งานภาคสนาม ด้วยเทคโนโลยีปัจจุบันทำให้มีเครื่องวัดสามารถตรวจวัดกรด-ด่างในของกึ่งแข็งได้เช่นอาหาร เนื้อสัตว์ พริกแกง และดิน ซึ่งเป็นประโยชน์ต่ออุตสาหกรรมในหลายด้าน


pH Meter คุณภาพสูง
มีสินค้าหลายรุ่นให้เลือกทั้งแบบปากกา ตั้งโต๊ะ สำหรับวัดในอุตสาหกรรม อาหาร เนื้อสัตว์ พริกแกง ผิวหนังและดิน เป็นต้น
คุณภาพสูงขายราคาถูก หลายรุ่นมีใบรับรอง Certificate of Analysis จากผู้ผลิต ดูรายละเอียดเพิ่มเติม
ความสำคัญของ pH
- ทางการเกษตร: โดยการกำหนดพีเอชของดิน เราสามารถหาได้ว่าเป็นกรดหรือด่าง ช่วยในการตัดสินใจเลือกชนิดของปุ๋ยที่จะใช้และชนิดของพืชที่จะหว่าน
- ในกระบวนการทางชีวภาพ: การรู้ค่าพีเอชทำให้เราสามารถปรับตัวกลางของกระบวนการทางชีวภาพ เช่น การหมัก เอนไซม์ไฮโดรไลซิส การฆ่าเชื้อ เป็นต้น
- ในการวิจัยการกัดกร่อน: โดยการวัดค่า pH ของน้ำทะเล จะศึกษาผลกระทบของน้ำทะเลที่เป็นด่างต่อวัสดุที่ใช้สร้างเรือและเรือดำน้ำ


